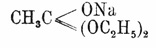
Ацетоуксусный эфир
и его гомологи, СН 3.СО.СН 2.СО 2 R, СН 3.СО.СНR.СО 2R, RCH2CO.CH2CO2 R, СН 3.СО.СR 2.CО 2 R и др., замечательные соединения, как по той роли, которую сыграло их изучение в развитии гипотезы таутомерии, так и по способности их вступать в целый ряд интересных и разнообразных реакций с неорганическими и органическими телами. А. эфир СН 3 СО.СН 2.СО 2 С 2 Н 5 открыт в 1863 г. Гейтером, получившим его действием металлического Na на уксусный эфир и давшим ему формулу β - оксикротонового эфира, СН 3.С(ОН):СН.СО 2 С 2 Н 5. Почти одновременно с Гейтером, Франкланд и Дюппа получили алкилзамещенный А. эфир действием Na и йодалкилов на уксусный эфир. Выяснение реакции образования и синтеза А. эфиров принадлежит Вислиценусу (1877), также Клайзену. Окончательно строение А. эфиров выяснено работами: Брюля, Конрада и Гаста (1898), Шиффа, Траубе (1895). Строение натр-А. эфиров установлено еще недостаточно точно. А. эфир получается при действии Na на 2CH 3CO2 R, при чем образуется сперва натр-А. эфир CH 3C(ONa):CH.CO2 R или CH 3CO.CHNa.CO2 R, этилат Na и выделяется водород. Из Na-A. эфиров самые эфиры получают разложением первых слабой кислотой. При действии этилата Na на 2СН 3 СООR тоже получается Na-A. эфир и C 2H5 ОН — но с меньшим выходом А. эфира (Клайзен). По Клайзену, эти реакции объясняются распадением Na-алкоголята ортоуксусного эфира,
— продукта прямого присоединения этилата Na — с другой частицей уксусного эфира:
CH3C(OC2H5)2 (ONa) + СН 3 СО 2 С 2 Н 5 = CH3.C(ONa):CH.CO2C2H5 + 2С 2 Н 5 ОН.
Образование А. эфиров помощью металлич. Na Клайзен объясняет предварительным образованием этилата (примесь спирта к уксусному эфиру), действующего дальше каталитически. В пользу этого говорят: 1) факт существования в свободном виде подобного же Na-ортопродукта этилового эфира бензойной кислоты; 2) Ладенбург (1870) показал, что обезвоженный и свободный от спирта CH 3CO2C2H5 совсем не реагирует с Na на холоду и лишь медленно — при нагревании; 3) при действии Na на смесь муравьиного эфира с другими эфирами или кетонами образуются продукты: CO 2 R.CH:CH(ONa) (Клайзен, 1898); 4) при действии Na на изомасляный эфир получается диизопропилщавелевый эфир (Барилович и С. Реформатский, 1895) (в реакцию синтеза А эфиров, по Клайзену, могут вступать лишь эфиры кислот, в которых С, связанный с карбоксилом, содержит по крайней мере два атома Н). Против объяснения Клайзена говорит тот факт, что Na реагирует с уксусным эфиром при низшей температуре и с лучшим выходом А. эфиров, чем Na-этилат, также — некоторая искусственность реакции распадения Na-ортоэфира с частицей уксусного эфира. Михаэль (1900) полагает, что сначала образуется Na-уксусный эфир, CH 2Na.CO2C2H5, реагирующий со второй частицей уксусного эфира с образованием:
который распадается на А. эфир и спирт. Однако, это объяснение встречает значительно больше возражений, чем — клайзеновское. Непонятны реакции синтеза А. эфиров с этилатом Na, с бензойным эфиром, не содержащим в α - положении водорода. Синтез А. эфира сразу же выяснил, что Na-A. эфирам можно придать двоякую формулу: или алкоголята β - оксикротонового эфира, или металлоорганического производного А.-эфиров. Этот вопрос открыт и теперь; А.-эфиры же — несомненно кетонные производные. Вопрос о таутомерии А. эфиров возник по почину Бутлерова, Кекуле, фан'т-Гоффа и Цинке и подробнее рассмотрен Лааром (1885—1893), также Брюлем (1894) и др. Лаар предложил рассматривать А. эфиры как смесь кетонной и энольной форм — структурных изомеров; атом водорода группировки.СО.СН 2. осциллирует между двумя положениями равновесия, обусловливая переход одной таутомерной формы в другую. Эта гипотеза подтверждена работами Клайзена, Гутцейта, Вислиценуса, фон Кнорра, П. Рабе и Р. Шиффа, установившими зависимость изомеризации от природы соединяющегося остатка, от температуры растворителя. На основании работ Брюля по оптическим свойствам А. эфиров (1894), Перкина (старшего, 1892) — по магнитному вращению, Друде (1897) — по диэлектрической постоянной, Траубе (1895) — по молекулярным объемам растворов, в А. эфирах должна быть принята кетонная форма строения, и гипотеза Лаара дополнена положением, что исходным пунктом изомеризации является кетонная форма А. эфиров. Кроме того, Конрад и Гаст (1898) нашли, что диметилтетроновая кислота,
кипит на 82° ниже, чем метилтетриновая,
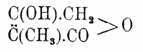 следовательно,
и диметил-А. эфир должен кипеть значительно ниже энольной формы монометил-А.
эфира. Нет оснований оспаривать энольную формулу для метилтетриновой кислоты.
Однако, диметил- и метил-А. эфиры разнятся в точках кипения всего на нисколько
градусов. Если бы гипотеза Лаара о смеси кетонной с энольной форм в А. эфире
была верна, то оба изомера можно было бы разделить фракционировкой. Это
рассуждение, однако, встречает возражение: быть может, при повышенной темп.
происходит полная изомеризация А. эфиров в энольную форму. Работа Шиффа (1898)
показала, что с бензальанилином А. эфир дает соединения, отвечающие как кетонной,
так и энольной формам; переход одной формы в другую Шифф осуществлял по
произволу. Однако, эта работа только лишний раз доказала способность А. эфиров к
изомеризациям в момент реакции. Таким образом, группировка R.CO.CH 2.CO.
легко переходит в R.C(OH):CH.CO.; чем сложнее группа R.CO, чем большими
электроотрицательными свойствами она обладает, тем легче такое тело переходит в
энольную форму (Клайзен). А. эфир СН 3 СО.СН 2 СО 2 С 2 Н 5
— приятно пахнущая жидкость, кипит при 181° (760 мм), D20
= 1,0256,
следовательно,
и диметил-А. эфир должен кипеть значительно ниже энольной формы монометил-А.
эфира. Нет оснований оспаривать энольную формулу для метилтетриновой кислоты.
Однако, диметил- и метил-А. эфиры разнятся в точках кипения всего на нисколько
градусов. Если бы гипотеза Лаара о смеси кетонной с энольной форм в А. эфире
была верна, то оба изомера можно было бы разделить фракционировкой. Это
рассуждение, однако, встречает возражение: быть может, при повышенной темп.
происходит полная изомеризация А. эфиров в энольную форму. Работа Шиффа (1898)
показала, что с бензальанилином А. эфир дает соединения, отвечающие как кетонной,
так и энольной формам; переход одной формы в другую Шифф осуществлял по
произволу. Однако, эта работа только лишний раз доказала способность А. эфиров к
изомеризациям в момент реакции. Таким образом, группировка R.CO.CH 2.CO.
легко переходит в R.C(OH):CH.CO.; чем сложнее группа R.CO, чем большими
электроотрицательными свойствами она обладает, тем легче такое тело переходит в
энольную форму (Клайзен). А. эфир СН 3 СО.СН 2 СО 2 С 2 Н 5
— приятно пахнущая жидкость, кипит при 181° (760 мм), D20
= 1,0256,
М Na = [p(n2—1)]/[d4(n2 + 2)] = 31,99 (Брюль).
Та же величина, вычисленная для кетонной формы = 31,78, а для энольной формы = 32,72. Замещенные А. эфиры и гомологи А. эфиров показали подобные же отношения рефрактометрических величин. А. эфир мало растворим в воде, перегоняется с водяным паром. Натр-А. эфир кристаллизуется в длинных иглах, растворим в эфире. Cu-A. эфир (Аллин, 1881) получается при смешении и взбалтывании уксуснокислой меди в эфирном растворе с А. эфиром. Он не растворим в воде, растворим в бензоле, эфире, плав. при 182°. Алюминий-А. эфир, плав. 80°, кипит 194° (8 мм) (Конрад, Тищенко, 1899). Магний-А. эфир, блестящие иголочки, темп. плав. 76°, возгоняются без разложения. Получены также Zn, Sn, Ni-соединения А. эфира (Конрад). Метил-А.-метиловый эфир СН 3 СОСН(СН 3)СО 2 СН 3, кипит 177°; диметил-А.-этиловый эфир кипит 184°. Приготовляется А. эфир (Вислиценус) так: в 2000 частях чистого уксусного эфира постепенно растворяют 60 ч. металл. натрия и отгоняют избыток СН 3 СО 2 С 2 Н 5. По остывании смесь этилата и Na-A. эфира затвердевает. Еще жидкую массу разлагают небольшим избытком 50% уксусной кислоты, при чем всплывает маслообразный слой; по отделении и просушке хлористым кальцием его фракционируют, при чем наибольшая фракция, переходящая при 175—185°, при повторной перегонке и дает А. эфир. Гомологи А. эфира получаются: 1) действием Na или его этилата — на эфиры отвечающих кислот: из эфира пропионовой кислоты получается эфир α - пропионилпропионовой кислоты; 2) реакцией натр-А. эфира с йод- и бромалкилами. Однозамещенный А. эфир способен давать Na-производное, которое позволяет ввести еще один остаток в частицу А. эфира:
CH.CO.CHNa.CO2R → CH3.COCHR' → CH3.CO.CNaR'.CO2R → CH3.CO.CR'R".CO2R
(Франкланд и Дюппа, Клайзен). Иногда можно вместо этилата Na в этой реакции взять NaOH (Гольдшмидт и Ослан, 1899); 3) действием FeCl 3 на хлорангидриды жирных кислот; при этом сперва образуются хлорангидриды кетонокислот, которые при действии спирта дают алкил-А. эфиры (Гамонэ, 1889):
4) цинк-галоидопроизводные жирных кислот (получены C. Реформатским и Г. Даиным, 1896) с нитрилами дают продукты присоединения, которые, по разложении водой, дают А. эфиры:
(Блэз, 1901). Mg-Gd-алкилы (Гриньяр, 1900) с цианоуксусным эфиром реагируют аналогично (Блэз, 1901).
Реакции А. эфиров: 1) с FeCl 3 — фиолетовое окрашивание; по Траубе, его дает только энольная форма А. эфиров; при низкой темп., также в бензоле, хлороформе, окраски нет; 2) образование бром-нитрозопродукта [Нейтральный водный раствор тела, в котором ищут СО-группу кетонов, смешивают с несколькими каплями раствора NH 2 (OH)HCl и прибавляют 5% раствора NaOH, каплю пиридина, немного (С 2 Н 5)2 О и затем прибавляют бромной воды, пока эфир не окрасятся в желтый или зеленый цвет. Наконец, приливают 1 куб. см раствора перекиси водорода, которая разрушает желтые соединения пиридина с Br, после чего, в присутствии СО-группы, обнаруживается синяя окраска.] — реакция Шток-Пилотти (1899). Превращения А. эфиров и их гомологов, частью ниже рассматриваемые, могут быть разделены на три категории: реакции распадения А. эфиров, замещения и уплотнения, или конденсации. С неорганическими телами ацетоуксусные эфиры реагируют главным образом по первому и второму типам; с органическими — по третьему типу. 1) Со щелочами: а) в слабом водном или спиртовом растворе, также — с баритовой водой, А. эфиры распадаются с образованием кетонов:
CH3.CO.(R)CH.CO2.C2H5 + 2КОН = RCH 2COCH2 + К 2 СО 3 + C2H5 ОН,
и b) — с образованием уксусной и алкилуксусных кисл. — при действии конц. спиртового КОН или этилата К:
CH.CO.RCHCO2C2H5 + 2КОН = СН 3.СО 2 К + RCH 2CO2K + C2H5OH.
А. эфир с водными щелочами и минеральными кислотами дает ацетон, СО 2 и спирт; с этилатом Na — ацетондикарбоновый эфир, C 2H5.СО 2.СН 2.СО.СН 2.СО 2.C2H5. С конц. Н 2 SО 4 А. эфир дает изодегидр-А. эфир,
Гомологи А. эфира, при нагревании с кислотами, дают кетон и СО 2. 2) При восстановлении водородом (амальг. Na) А. эфиры дают β - оксикислоты и обмыливаются. 3) Действием Cl и Вr на А. эфиры получаются галоид-А. эфиры, при чем замещается Н, как группы СН 2, так и СН 3. Хлор замещает сперва Н в СН 2 -группе, Вr — наоборот. С йодом Na-A. эфир дает диацетоянтарный эфир,
это тело образуется также при электролизе А. эфира. 4) С PCl 5 получается хлорангидрид ββ - дихлор-А. эфира, СН 3 ССl 2 СН 2 СОСl. 5) Действием аммиака, анилина, гидразина, фенилгидразина, семикарбазида на ацетоуксусный эфир получаются: имиды, анилы, гидразоны, фенилгидразоны, семикарбазоны. Эти продукты тождественны с такими же β - производными эфиров кротоновой кислоты [Литература: Колли (1885), Оппенгейм и Прехт (1876), Кнорр (1884), Ридель (1896), Эбштейн (1885), Неф и Икута (1891). Последние авторы стоят за энольную форму для А. эфира, но все реакции, приводимые ими в доказательство, отлично объясняются и с точки зрения кетонной формы.]. Метилфенилгидразин с А. эфиром дает антипирин (см. Пирроазолы). 6) С гидроксиламином все А. эфиры дают эфиры β - изонитрозожирных кислот, которые далее легко переходят в изоксазолоны (см. Фуразолы). 7) Азотистая кислота дает с А. эфирами изонитрозосоединения CH 3.CO.C(:N.OH)CO2 R, легко распадающиеся на изонитрозоацетон, СО 2 и спирт. Моноалкил-А. эфиры с HNO 2 дают α - изонитрозожирные кислоты, отщепляя СН 3 СО, a соответствующие свободные кислоты отщепляют еще и СО 2 и дают кетоны. Подобно HNO 2 реагируют с А. эфиром соли ароматических диазониев. 8) Диазометан (см.) переводит А. эфир в β - метоксицискротоновый эфир, СН 3 С(ОСН 3):СН.СО 2 Н — пример полной изомеризации А. эфира в энольную форму. 9) С фенолами и H 2 SО 4 А. эфиры конденсируются в кумарины (см.). 10) С альдегидами, напр. ацетальдегидом, А. эфир конденсируется в этилиденмоно- и этилиден-бис-А. эфиры. Последние, γ - дикетоны,
с выпадением воды дают производные кетогидробензола,
(Кневенагель, 1895); с NH 3 А. эфиры конденсируются в производные гидропиридинов (Клайзен, 1882). С ацетоном А. эфир уплотняется, при действии водуотнимающих веществ, в изопропилиден-А. эфир, СН 3.СО.С(СО 2 С 2 Н 5):С(СН 3)2 (Поби, 1897). 11) С хлорангидридами кислот натр-А. эфир может дать три ряда производных: а) с хлорангидридным остатком у α - углеродной группы — α - ацил-А. эфир, b) с тем же остатком у кислорода β - карбонильной группы — β - ацил-А. эфир и с) с тем же остатком у обеих групп одновременно — αβ - ацил-А. эфир (αα - ацил-А. эфиры не образуются). Реакция изучена Клайзеном над действием хлористого бензоила на А. эфир. 12) С CHCl 2 А. эфир дает оксиувитиновую кислоту, С 6 Н 2 (СН 3)(ОН)(СО 2 Н) 2 (Оппенгейм и Прехт, 1876). 13) С мочевиной А. эфир дает метилурацил — исходное вещество для синтеза мочевой кислоты (см.). 14) Амидины (см.) дают с А. эфиром оксипиримидины.
П. Григорович.