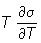 ,
,Поверхностная энергия в термодинамике, избыток энергии в тонком слое вещества у поверхности соприкосновения тел (фаз) по сравнению с энергией вещества внутри тела. Полная П. э. складывается из работы образования поверхности, т. е. работы, необходимой для преодоления сил межмолекулярного (или межатомного) взаимодействия при перемещении молекул (атомов) из объёма фазы в поверхностный слой, и теплового эффекта, связанного с этим процессом. В соответствии с термодинамическими зависимостями удельная полная П. э.
u = s + q = s —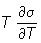 ,
,
где s — удельная свободная П. э., тождественно равная для подвижных жидкостей поверхностному натяжению, q — скрытая теплота (связанная энергия) единицы площади поверхности, Т — абсолютная температура и 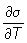 — удельная поверхностная энтропия, имеющая обычно отрицательную величину. Свободная П. э. с ростом температуры уменьшается, тогда как полная П. э. неполярных (неассоциированных) жидкостей остаётся постоянной, а полярных — несколько возрастает. Так, для воды при 0, 20 и 100 °С значения u соответственно равны 117, 120 и 129 мдж/м2 или эрг/см2. С приближением к критической температуре различие в составе и свойствах контактирующих фаз сглаживается, поверхность раздела фаз исчезает и П. э. обращается в нуль. П. э. влияет на многие физико-химические свойства твёрдых тел и жидкостей. Особенно возрастает её роль в высокодисперсных коллоидных системах, где поверхность раздела фаз предельно велика.
— удельная поверхностная энтропия, имеющая обычно отрицательную величину. Свободная П. э. с ростом температуры уменьшается, тогда как полная П. э. неполярных (неассоциированных) жидкостей остаётся постоянной, а полярных — несколько возрастает. Так, для воды при 0, 20 и 100 °С значения u соответственно равны 117, 120 и 129 мдж/м2 или эрг/см2. С приближением к критической температуре различие в составе и свойствах контактирующих фаз сглаживается, поверхность раздела фаз исчезает и П. э. обращается в нуль. П. э. влияет на многие физико-химические свойства твёрдых тел и жидкостей. Особенно возрастает её роль в высокодисперсных коллоидных системах, где поверхность раздела фаз предельно велика.
Лит. см. при ст. Поверхностное натяжение и Поверхностные явления.
Л. А. Шиц.