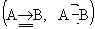
Тройная связь, химическая ковалентная связь, осуществляемая тремя парами электронов, находящихся в поле двух атомных ядер. Т. с. включает одну s- и две p-связи (см. Сигма- и пи-связи); результирующее распределение электронной плотности между двумя связанными ядрами имеет осевую симметрию (как в случае простой связи). В структурных формулах химических соединений Т. с. между атомами обозначается тремя валентными штрихами, например N º N, С º С, C º N. Если одна или обе p-компоненты Т. с. (например, между атомами А и В) образуются в результате донорно-акцепторного взаимодействия (см. Донорно-акцепторная связь), такие Т. с.
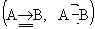
обычно называют квазитройными (в «нормальной» Т. с. А º В s и две p-компоненты образованы в результате взаимодействия неспаренных электронов). Примеры квазитройных связей: связь концевого атома кислорода с атомом переходного металла ( , так называемая «иловая» связь), например в K2[ReOCI5], связь в молекуле
, так называемая «иловая» связь), например в K2[ReOCI5], связь в молекуле
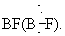
Вследствие большой энергии Т. с. и квазитройных связей соответствующие молекулы (например, N2, CO) или молекулярные фрагменты (например, N º Me,  ) термодинамически устойчивы и обычно химически инертны. Так, фиксация молекулярного азота (то есть активация его для химических превращений) невозможна без предварительной координации его как лиганда в определённых комплексах переходных металлов, в результате которой кратность (прочность) связи азот — азот существенно уменьшается.
) термодинамически устойчивы и обычно химически инертны. Так, фиксация молекулярного азота (то есть активация его для химических превращений) невозможна без предварительной координации его как лиганда в определённых комплексах переходных металлов, в результате которой кратность (прочность) связи азот — азот существенно уменьшается.
Если раньше в основном изучались Т. с. между лёгкими атомами (С, N), то теперь всё большее внимание уделяется Т. с. с участием тяжёлых атомов, прежде всего атомов переходных металлов; эти тройные связи реализуются в новых типах комплексных соединений. Уже изучено большое число комплексных соединений переходных металлов с нитридо (N º )–, оксо  , имино
, имино 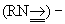 и карбиновыми (RC º ) группами как лигандами, характеризующимися высокой прочностью химических связей. Важной особенностью указанных лигандов является их сильное трансвлияние (то есть сильное ослабление связи металл — лиганд в транспозиции), что предопределяет многие свойства и реакционную способность таких соединений. Кроме того, известны димерные кластеры переходных металлов с Т. с. металл — металл, например Mo2[N (CH3)2]6. Эта молекула имеет центросимметричную повёрнутую (как в этане C2H6) конфигурацию, что обусловлено осевой симметрией распределения электронной плотности в связи Me º Me, где Me — металл. См. также Валентность, Химическая связь.
и карбиновыми (RC º ) группами как лигандами, характеризующимися высокой прочностью химических связей. Важной особенностью указанных лигандов является их сильное трансвлияние (то есть сильное ослабление связи металл — лиганд в транспозиции), что предопределяет многие свойства и реакционную способность таких соединений. Кроме того, известны димерные кластеры переходных металлов с Т. с. металл — металл, например Mo2[N (CH3)2]6. Эта молекула имеет центросимметричную повёрнутую (как в этане C2H6) конфигурацию, что обусловлено осевой симметрией распределения электронной плотности в связи Me º Me, где Me — металл. См. также Валентность, Химическая связь.
Лит.: Шусторович Е. М., Химическая связь, М., 1973.
Е. М. Шусторович.